Our Institute
Clinical Trials
Our Science
News
International Patients
- International Patients
- International patient Service Care
- Travel Arrangement and Hospital Admission
- FAQ
- Contact Us
恶性脑胶质瘤, WHO分级2级以上的都归类于恶性胶质瘤,从目前的文献报道,2级以上的脑胶质瘤复发率接近100%,而其中恶性程度极高的GBM(胶质母细胞瘤,WHO分级4级)的中位总生存期低于14.6月,而好发于儿童的弥漫性中线胶质瘤(包括DIPG)更是给家庭带来极大的痛苦。近20年来,尽管采用手术,化疗、放疗、物理治疗以及靶向药,效果仍然不显著,恶性胶质瘤的临床治疗急需新的方法与突破。
免疫疗法正迅速成为治疗恶性肿瘤的新希望。原来中枢神经系统被认为不存在淋巴系统,是免疫特权区。然而,最近发现,中枢神经系统中依然存在着淋巴系统,因此有了对脑部肿瘤逃避免疫系统监控机制的新见解,也对脑癌免疫治疗产生了新的希望。
深圳市免疫基因治疗研究院开展抗原特异性T细胞治疗多年,现在针对弥漫内生性脑桥神经胶质瘤(DIPG)与脑胶质瘤(GBM)的临床试验,已通过临床伦理委员会 (http://www.szgimi.org, GIMI-IRB-17003, GIMI-IRB-19001)与国际临床试验网(https://www.clinicaltrials.gov) 登记注册 (NCT:03170141, NCT03914768),并和南方医科大学深圳医院( http://www.smuszh.com) 展开合作。并已进行第一例脑瘤CART靶向细胞注射治疗,引领国际免疫细胞治疗水平。
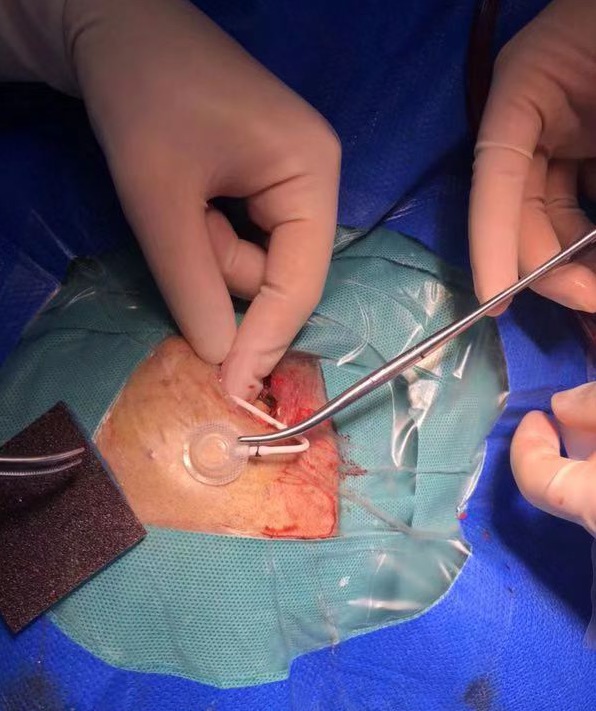
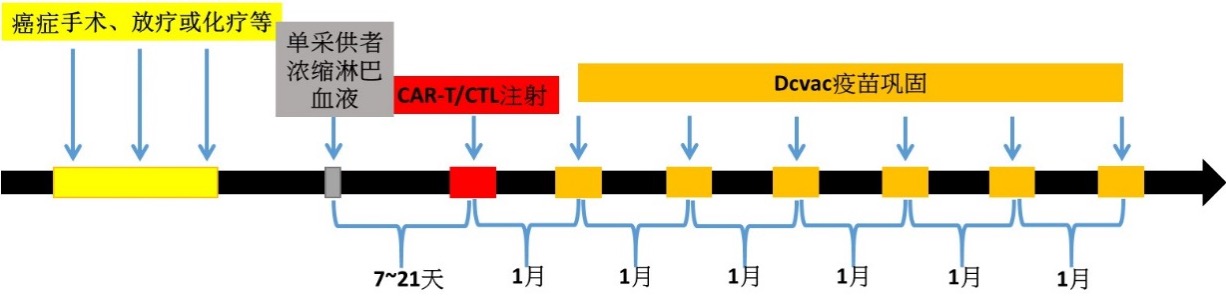
临床试验流程:
根据患者脑瘤特异性靶点,采用自身的免疫细胞,经体外改造成表达免疫调控基因的抗脑瘤抗原特异性T细胞,合并使用抗原特异性CTL(CAR-T/CTL),与免疫修饰树突状细胞疫苗 (DCvac) 整合治疗脑瘤,相关技术介绍请参考GIMI研究院网页 (http://www.szgimi.org)。依据肿瘤治疗经验与理论,即使初步治疗看到肿瘤缩小或是完全消失,体内残留的微小肿瘤细胞或是肿瘤干细胞,仍然可能复发或是转移到其它组织器官。因此,后续治疗必须着重于提升抗肿瘤免疫力。临床实验设计包含后续DCvac的应用,以避免复发与肿瘤转移。 本临床试验提出一贯性的免疫治疗临床实验方案,仍须进一步评估不同免疫靶点的安全性与有效性。
临床入组条件:
(1) 年龄>6个月,<80足岁;
(2) 临床病理资料证实为恶性胶质瘤;
(3) 癫痫症状已获得良好控制;
(4) 经免疫表型分析、细胞学、基因学检测后,具有本试验中所提到的抗原特异表现,或是无检体分析但是符合已知预期相关肿瘤抗原;
(5) KPS (Karnofsky) 功能状态评分标准评分在60分以上;
(6) 重要脏器功能满足:心脏超声提示心脏射血分数≥50%,心电图未见明显异常;血氧饱和度≥90%;肌酐≤2.5倍正常值范围;ALT(谷丙转氨酶)和AST(谷草转氨酶)≤3倍正常值范围,总胆红素≤2.0mg/dl;
(7) Hgb(血红蛋白)≥80g/L;
(8) 外周血淋巴细胞数大于0.8x10^9/L且无单采及细胞分离禁忌症;
(9) 患者及家属有强烈的参与临床试验意愿,且愿意承担试验的一切风险,并签署知情同意书;
(10) 经专家组讨论分析患者病情,结合患者一般身体状况,认为参与该项临床试验获益大于风险。
患者诊疗流程:
1. 患者将自身完整的病历资料进行电子档整理并发送至公众号邮箱,需要包括疾病的主要发病历程及治疗方案、已进行过的治疗手段,以及最近的影像学检查结果报告及医院拷贝的原始文件(如适用),需注明是否进行过免疫细胞治疗。
2. 专家组与患者及家属双方同意进行靶点筛查,患者提供肿瘤组织白片(15-20片)或蜡块样本,染色结果确定表达高的特异靶点抗原后,即可拟定治疗方案。
3. 根据患者提供的信息,由专家组评估是否符合医院伦理及临床试验入组条件,符合入组的患者签署知情同意书后进行治疗。
4. 可在北京或深圳进行淋巴细胞采集,免疫细胞制剂制备时程;CAR-T制备约1周,EIE(CTL)制备约1个月,癌症疫苗制备约1周。
5. 注射前需在医院进行治疗前观察及化疗预处理,细胞注射后须配合随访人员,定期记录追踪临床数据。
咨询方式:
如希望了解更多的信息或有兴趣参与本研究,请与我们的工作人员联系,他(她)将更为详细地介绍本研究,并安排您进行相应的检查与安排入组治疗。亦可通过深圳市免疫基因治疗研究院官方网站,微信公众号、既往患者或医生专家推荐等形式了解相关信息,进行电话咨询或微信公众号留言咨询。
官方网站:http://www.szgimi.org/
咨询电话:0755-86725195
微信公众号:szgimiirb
资料上传邮箱:gimi_trials@szgimi.org